Lityum pil hücresi bulamaç karıştırma, tüm üretim sürecindeki en önemli bağlantıdır ve bu, lityum iyon pilin tüm üretim sürecindeki en önemli bağlantıdır.
Lityum iyon pil için pozitif elektrot bulamacının bileşimi
Lityum iyon pilin pozitif elektrot bulamacı, bağlayıcı, iletken ajan, pozitif elektrot malzemesi vb. negatif elektrot bulamacı, bağlayıcı, grafit karbon tozu vb.'den oluşur. Pozitif ve negatif bulamaçların hazırlanması, sıvı ve sıvı, sıvı ve katı malzemeler arasında karşılıklı karıştırma, çözme ve dağıtma gibi bir dizi teknolojik işlemi içerir ve bu işlemler, Sıcaklık, viskozite ve ortamdaki değişiklikler eşlik eder. Pozitif ve negatif elektrot bulamaçlarında, granüler aktif malzemenin dağılımı ve homojenliği, pilin iki kutbu arasındaki lityum iyonlarının hareketini doğrudan etkiler, bu nedenle her bir kutup parçası malzemesinin bulamacının karıştırılması ve dağılması çok önemlidir. lityum iyon pillerin üretimi. , Bulamaç dağılımının kalitesi, sonraki lityum iyon pil üretiminin kalitesini ve ürünlerinin performansını doğrudan etkiler.
Geleneksel işlemde, ultra ince dağılım gerçekleştirilir çünkü: geleneksel karıştırma ve karıştırma ekipmanı aracılığıyla, çözeltideki yalnızca büyük toz kümeleri dağıtılabilir ve eşit olarak dağıtılabilir; bununla birlikte toz formu, ince toz kümeleri şeklinde mevcuttur. Çözümde, yalnızca makroskopik dağılımın işleme gereksinimleri karşılanmaktadır. Makroskopik karıştırma ve dispersiyondan sonra bulamaç, yeterince ince katılar elde etmek için ultra-ince dispersiyon ve homojenleştirme ekipmanının güçlü mekanik kesme kuvvetinin etkisi altında çözeltideki ince toz veya katı parçacık aglomeratlarını daha da dağıtabilir ve homojenleştirebilir. Parçacıklar, bulamacın kapsamlı performansını önemli ölçüde artırabilen mikroskobik ultra ince dağılım ve homojenliğin etkisini elde etmek için çözelti içinde eşit olarak dağıtılır.
Mevcut geleneksel lityum pil bulamaç süreci:
malzemeler
- Çözüm hazırlığı:
a) PVDF (veya CMC) ve solvent NMP'nin (veya deiyonize suyun) karışım oranı ve tartımı;
b) Çözeltinin karıştırma süresi, karıştırma sıklığı ve süreleri (ve çözeltinin yüzey sıcaklığı);
c) Çözeltinin hazırlanması tamamlandıktan sonra çözeltinin incelenmesi: viskozite (test), çözünme derecesi (görsel inceleme) ve raf süresi;
d) Negatif elektrot: SBR+CMC solüsyonu, karıştırma süresi ve sıklığı.
Aktif maddeler:
a) Tartım ve karıştırma sırasında, karıştırma oranı ve miktarının doğru olup olmadığını izleyin;
b) Bilyeli öğütme: pozitif ve negatif elektrotların bilyeli öğütme süresi; bilyalı öğütme tamburundaki karışıma akik boncuk oranı; akik toplarda büyük topların küçük toplara oranı;
c) Pişirme: pişirme sıcaklığının ve süresinin ayarlanması; Pişirmeden sonra soğuduktan sonra test sıcaklığı.
d) Aktif madde ve çözeltinin karıştırılması ve karıştırılması: karıştırma modu, karıştırma süresi ve sıklığı.
e) Elek: 100 gözlü (veya 150 gözlü) moleküler elekten geçirin.
f) Test, muayene:
Bulamaç ve karışım üzerinde aşağıdaki testler gerçekleştirilir: katı içerik, viskozite, karışım inceliği, musluk yoğunluğu ve bulamaç yoğunluğu.
Geleneksel işçiliği açıklığa kavuşturmanın yanı sıra, lityum pil bulamacının temel ilkelerini de anlamak gerekir.
kolloid teorisi
Kolloidal partiküllerin aglomerasyonuna yol açan ana etki, partiküller arasındaki van der Waals kuvvetidir. Kolloidal partiküllerin stabilitesini arttırmak için iki yol vardır: biri kolloidal partiküller arasındaki elektrostatik itmeyi arttırmak, diğeri ise tozlar arasında sterik potansiyeller oluşturmaktır. Bu iki yolla tozun aglomerasyonu bloke edilir.
En basit kolloidal sistem, dağılmış bir faz ve dağılmış bir ortamdan oluşur ve dağılmış fazın boyutu 10-9 ila 10-6 m arasında değişir. Kolloiddeki maddeler sistemde bulunur ve belirli bir derecede dağılabilirliğe sahip olmaları gerekir. Çözücü ve dağılmış faz arasındaki farka göre, çeşitli kolloid formlar üretilebilir, örneğin: sis, damlacıkların gaz içinde dağıldığı aerosoldur, katı polimer parçacıklarının sıvı içinde dağıldığı diş macunu soldur.
Kolloidlerin yaşamda birçok uygulaması vardır ve kolloidlerin fiziksel özellikleri, dağılım fazına ve dağılım ortamına bağlı olarak değişir. Kolloidleri mikroskobik bir bakış açısıyla incelersek, kolloidal parçacıklar sabit bir durumda değildir, ancak ortam içinde rastgele hareket ederler, buna Brown hareketi diyoruz. Mutlak sıfırın üzerinde, kolloidal parçacıklar, mikroskobik kolloidlerin dinamik özellikleri olan termal hareket nedeniyle Brownian hareketine uğrayacaktır. Brownian hareketi nedeniyle kolloidal parçacıkların çarpışması, kümelenme için bir fırsattır ve kolloidal parçacıklar termodinamik olarak kararsız bir durumdadır, bu nedenle parçacıklar arasındaki etkileşim kuvveti, dağılmanın temel faktörlerinden biridir.
Elektrikli çift katman teorisi
Elektrik çift katman teorisi, kolloidlerdeki yüklü iyonların dağılımını ve parçacıkların yüzeyindeki potansiyel sorunları açıklamak için kullanılabilir. 19. yüzyılda Helmholtz, elektrikli çift katmanlı yapıyı tanımlamak için paralel kapasitör modelini önerdi. Basitçe, parçacıkların negatif yüklü olduğu ve yüzeyin bir kapasitördeki elektrot gibi olduğu varsayılır. Ancak bu teori, termal hareket nedeniyle yüklü iyonların difüzyon davranışını göz ardı eder.
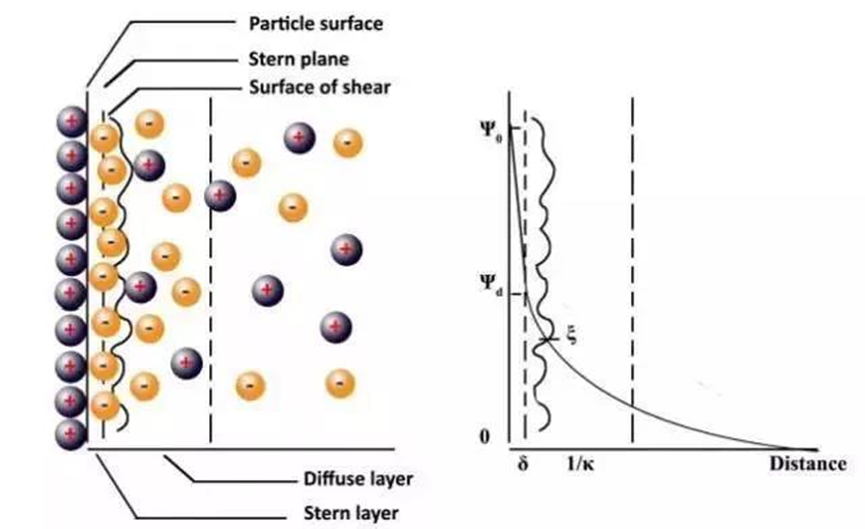
Bu nedenle, 20. yüzyılın başlarında Gouy ve Chapman, çözeltideki karşı iyonların elektrostatik etkileşim nedeniyle yüklü parçacıkların yüzeyinde adsorbe olacağı ve aynı zamanda, elektriksel çift katmanlı difüzyon modelini önerdiler. termal hareket nedeniyle parçacıkların etrafında yayılır. Bu nedenle, çözeltideki karşı iyonların dağılım konsantrasyonu parçacık yüzeyinden uzaklaştıkça azalacaktır. 1924'te Stern, elektrikli çift katmanın yapısını tanımlamak için iki paralel kapasitör ve dağınık elektrik çift katmanı modelini birleştirdi. Stern, karşı iyonların partikülün yüzeyinde Stern tabakası olarak da bilinen sıkı bir adsorpsiyon tabakası oluşturacağına inanmaktadır. Parçacık yüzeyinden uzaklık arttıkça parçacığın potansiyeli lineer olarak azalacaktır. Aynı zamanda, Stern tabakasının dışında bir difüzyon tabakası da vardır ve partiküller difüzyona uğrayacaktır. Tabakadaki potansiyel, mesafe ile katlanarak azalır.
Aşağıdaki şekil, Stern elektrikli çift katmanlı modelini göstermektedir. Zeta potansiyeli (ξ, Zeta potansiyeli), elektrikli çift katmanlı modelde çok önemli bir parametredir. Parçacığın yüzey potansiyeli gerçek ölçümde doğrudan ölçülemez, ancak akustik dalga yöntemi veya elektroforez yöntemi ile hesaplanabilir. parçacığın zeta potansiyeli. Zeta potansiyeli, elektrikli çift katmanlı modelde Stern katmanı ile difüzyon katmanı arasındaki kesme düzleminde bulunur.
Zeta potansiyeli, kolloidin dağılma stabilitesi ile yakından ilişkilidir. Zeta potansiyeli daha büyük olduğunda, kolloid partikülün yüzeyindeki elektrostatik yük daha fazladır. Partikülün sulu çözeltideki zeta potansiyeli ±25~30mV'ye ulaştığında, kolloid, kolloidal kararlılığı korumak için partiküller arasındaki van der Waals kuvvetlerinin üstesinden gelmek için yeterli Elektrostatik itme gücüne sahiptir.
DLVO teorisi
1940'tan 1948'e kadar Deryagin, Landau, Verwey, Overbeek, kolloidal parçacıklar birbirine yaklaştığında enerji değişimi ve bunun DLVO teorisi olarak adlandırılan kolloidal stabilite üzerindeki etkisi ile ilgili teoriyi kurdu. Teorisi temel olarak kolloidal parçacıklar arasındaki mesafe ile enerji değişimi arasındaki ilişkiyi tanımlar.
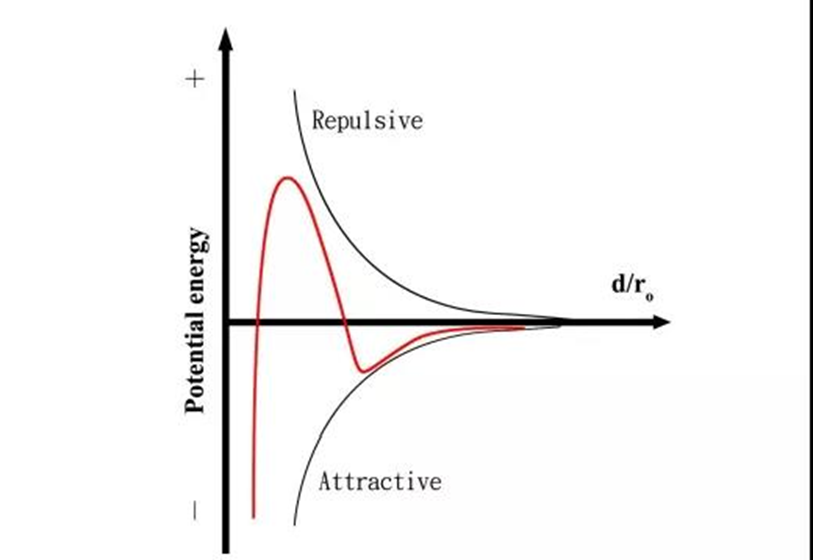
Aşağıdaki şekil, kolloidal parçacıklar arasında çekici ve itici güçler olduğunu gösteren DLVO'nun şematik bir diyagramıdır. Bu iki kuvvetin boyutu, kolloidal çözeltinin kararlılığını belirler. Parçacıklar arasındaki çekim ana etkidir ve parçacıklar topaklanacaktır; itici kuvvet Çekici kuvvetten daha büyük durumdayken, partikül kohezyonu önlenebilir ve kolloidin stabilitesi korunabilir.
DLVO eğrisinden, tanecikler arası mesafe kısaldıkça tanecikler önce birbirini çekecek, tanecikler birbirine yaklaşmaya devam ederse tanecikler arasında itme kuvveti oluşacak, tanecikler birbirini keserse önce tanecikler birbirini çekecektir. itme bariyeri, Agregalar hızla. Bu nedenle, kolloidlerdeki partiküllerin dağılım stabilitesini iyileştirmek için partiküller arasında topaklaşmayı önlemek için partiküller arasındaki itme kuvveti geliştirilmelidir.
Kolloid stabilizasyon mekanizması
Kolloidal parçacıklar, yüksek yüzey enerjilerinden dolayı topaklanma eğilimindedir. Kolloidal sistemin dispersiyon stabilitesine sahip olması için partiküller arasındaki itme kuvvetinin iyileştirilmesi gerekir. Kolloidler arasındaki stabilizasyon mekanizması genel olarak üç tipe ayrılabilir:
1) Elektrostatik stabilizasyon
2) Sterik engelleme
3) Elektrosterik stabilizasyon, stabilizasyon mekanizması aşağıdaki şekilde gösterilmiştir:
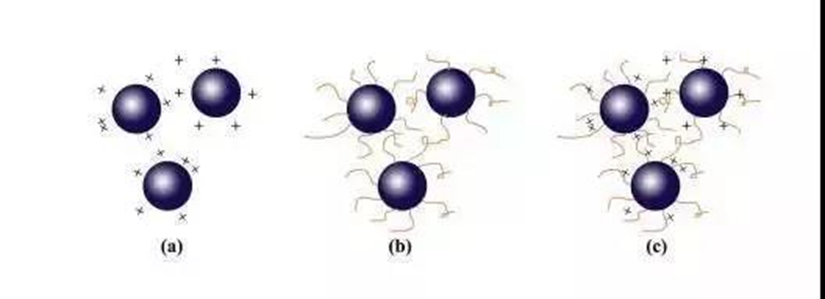
(a) elektrostatik itme, (b) sterik bariyer, (c) elektrostatik sterik bariyer
Elektrostatik stabilizasyon mekanizması, parçacıkların yüzey yüklerinin neden olduğu itme kuvvetini kullanır. Parçacıklar çekim nedeniyle birbirine yakın olduğunda, kolloidal parçacıkların elektriksel çift katmanları üst üste biner ve parçacıkların yüzeyinde aynı yük nedeniyle itme kuvveti üretilir.
Ancak elektrostatik stabilizasyon mekanizması, çözelti sistemindeki elektrolit konsantrasyonundan kolaylıkla etkilenir. Çözeltideki elektrolit konsantrasyonu çok yüksek olduğunda, parçacıkların yüzeyindeki elektrikli çift tabaka sıkıştırılacak ve bu da parçacıkların yığılmasına neden olacaktır. Sterik bariyerlerin stabilizasyon mekanizması, partiküller arasındaki itme kuvvetini arttırmak için iki farklı etki üretecek olan kolloidal partiküllerin yüzeyinde adsorbe etmek için makromoleküller kullanmaktır:
1) Ozmotik Etki
İki koloidal partikül birbirine yakın olduğunda, partiküllerin yüzeyine adsorbe edilen uzun zincirli polimer veya çözeltideki kalıntı polimer partiküller arasına yerleştirilecektir. Bu sırada, partiküller arasındaki polimer konsantrasyonunun sürekli artışı, ozmotik basıncın değişmesine neden olacak ve çevreleyen ortam iki koloidal partikül içine girecektir. Parçacıklar arasında, kararlı dağılım etkisini elde etmek için birbirinden uzaklık düzenlenir.
2) Hacim kısıtlama etkisi
Makromolekülün partikülün üst yüzeyinde adsorbe edilmesi için belirli bir boşluk bariyeri vardır. Parçacıklar arasındaki mesafe kısaltıldığında, makromolekül parçacığa nüfuz edemediğinden, makromolekül sıkıştırılacak, bu da elastik serbest enerjide bir artışa neden olacak, böylece parçacığın yerini alacak ve dispersiyon etkisi elde edilecektir. .
Elektrostatik stabilizasyon mekanizmalarıyla karşılaştırıldığında, polimerik sterik bariyerlerin birçok avantajı vardır. Elektrostatik stabilizasyon mekanizması ortamdan kolayca etkilenir ve etkisini kaybeder, elektroliti yüksek ortamlara veya organik sistem solüsyonlarına uygulanamaz.
Bununla birlikte, makromoleküler sterik bariyerler elektrolit konsantrasyonuna nispeten duyarsızdır ve sulu çözeltide veya organik çözücülerde aynı etkinliğe sahiptir ve makromoleküler sterik bariyerler, kolloidal katı içeriğinden dolayı etkiyi etkilemez. Polimer kolloidal parçacıkların yüzeyinde adsorbe edildiğinde, aglomerasyon meydana gelse bile, aglomerasyon fenomenini kolayca kırabilen yumuşak aglomerasyondur. Kolloidal partiküller kurutulsa bile yine solvent içinde dağılabilirler.
Bu nedenle, sterik bariyerlerin dağılım stabilitesi üzerindeki etkisi, elektrostatik stabilizasyondan nispeten daha yüksektir. Elektrostatik sterik stabilizasyon, hem elektrostatik stabilizasyon mekanizmasına hem de sterik bir bariyere sahiptir. Parçacığın yüzeyine aşılanmış polimer yüklenir, böylece iki farklı stabilizasyon mekanizması eklenir, böylece koloidal parçacıklar iyi bir dağılım kararlılığına sahip olur.
Keheng New Energy'nin Ürün Yelpazesi
- 100AH 12V Düşük Sıcaklık Isıtma Etkin
- Lityum Pil Hücresi
- Lityum Pil Paketi
- Escooter/Ebike Pil
- 12V/24V Lifepo4 Pil
- Taşınabilir Güç İstasyonu
- ESS Enerji Depolama Sistemleri
- BMS'li Derin Döngü Piller
- Düşük Sıcaklık 24V 60AH Pil