La agitación de lodos de celdas de batería de litio es el eslabón más importante en todo el proceso de producción, que es el eslabón más importante en todo el proceso de producción de la batería de iones de litio.
Composición de la suspensión de electrodo positivo para batería de iones de litio
La suspensión de electrodo positivo de la batería de iones de litio está compuesta de aglutinante, agente conductor, material de electrodo positivo, etc.; la suspensión del electrodo negativo se compone de aglutinante, polvo de carbón de grafito, etc. La preparación de las suspensiones positivas y negativas incluye una serie de procesos tecnológicos como la mezcla mutua, la disolución y la dispersión entre líquido y líquido, materiales líquidos y sólidos, y estos procesos son acompañada de cambios en la temperatura, la viscosidad y el medio ambiente. En las lechadas de electrodo positivo y negativo, la dispersión y uniformidad del material granular activo afecta directamente el movimiento de los iones de litio entre los dos polos de la batería, por lo que la mezcla y dispersión de la lechada de cada material de la pieza polar es muy importante en la producción de baterías de iones de litio. , La calidad de la dispersión de la suspensión afecta directamente la calidad de la producción posterior de baterías de iones de litio y el rendimiento de sus productos.
En el proceso tradicional, la dispersión ultrafina se lleva a cabo porque: a través del equipo tradicional de mezcla y agitación, solo se pueden dispersar y distribuir uniformemente grandes grupos de polvo en la solución; sin embargo, la forma de polvo existe en forma de racimos de polvo fino. En la solución, solo se cumplen los requisitos de procesamiento de la dispersión macroscópica. La suspensión después de la agitación macroscópica y la dispersión puede dispersar y homogeneizar aún más el polvo fino o los aglomerados de partículas sólidas en la solución bajo la acción de la fuerte fuerza mecánica de corte del equipo de dispersión y homogeneización ultrafina para obtener sólidos suficientemente finos. Las partículas se distribuyen uniformemente en la solución para lograr el efecto de dispersión ultrafina microscópica y homogeneidad, lo que puede mejorar significativamente el rendimiento integral de la suspensión.
El actual proceso tradicional de suspensión de baterías de litio es:
Ingredientes
- Preparación de la solución:
a) La relación de mezcla y el peso de PVDF (o CMC) y solvente NMP (o agua desionizada);
b) El tiempo de agitación, la frecuencia y los tiempos de agitación de la solución (y la temperatura superficial de la solución);
c) Una vez completada la preparación de la solución, la inspección de la solución: viscosidad (prueba), grado de disolución (inspección visual) y tiempo de almacenamiento;
d) Electrodo negativo: solución SBR+CMC, tiempo y frecuencia de agitación.
Sustancias activas:
a) Al pesar y mezclar, controlar si la relación de mezcla y la cantidad son correctas;
b) Molienda de bolas: el tiempo de molienda de bolas de los electrodos positivo y negativo; la relación entre las perlas de ágata y la mezcla en el cilindro de molienda de bolas; la proporción de bolas grandes a bolas pequeñas en las bolas de ágata;
c) Horneado: configuración de la temperatura y del tiempo de horneado; temperatura de prueba después de enfriar después de hornear.
d) Mezcla y agitación de la sustancia activa y la solución: modo de agitación, tiempo y frecuencia de agitación.
e) Tamiz: pasar a través de un tamiz molecular de malla 100 (o malla 150).
f) Pruebas, inspección:
Se llevan a cabo las siguientes pruebas en la lechada y la mezcla: contenido de sólidos, viscosidad, finura de mezcla, densidad del golpe y densidad de la lechada.
Además de aclarar la artesanía tradicional, también es necesario comprender los principios básicos de la suspensión de baterías de litio.
Teoría de los coloides
El principal efecto que lleva a la aglomeración de partículas coloidales es la fuerza de van der Waals entre partículas. Para aumentar la estabilidad de las partículas coloidales, hay dos formas: una es aumentar la repulsión electrostática entre las partículas coloidales y la otra es generar potenciales estéricos entre los polvos. De estas dos formas se bloquea la aglomeración del polvo.
El sistema coloidal más simple está compuesto por una fase dispersa y un medio disperso, y el tamaño de la fase dispersa varía de 10-9 a 10-6 m. Las sustancias del coloide existen en el sistema y necesitan tener un cierto grado de dispersabilidad. De acuerdo con la diferencia del solvente y la fase dispersa, se pueden producir varias formas coloidales, tales como: la niebla es un aerosol en el que las gotas se dispersan en gas, la pasta de dientes es un sol en el que las partículas sólidas de polímero se dispersan en un líquido.
La aplicación de coloides abunda en la vida, y las propiedades físicas de los coloides varían según la fase de dispersión y el medio de dispersión. Observando los coloides desde un punto de vista microscópico, las partículas coloidales no están en un estado constante, sino que se mueven aleatoriamente en el medio, que es lo que llamamos movimiento browniano. Por encima del cero absoluto, las partículas coloidales sufrirán un movimiento browniano debido al movimiento térmico, que son las características dinámicas de los coloides microscópicos. La colisión de partículas coloidales debido al movimiento browniano es una oportunidad para la agregación, y las partículas coloidales se encuentran en un estado termodinámicamente inestable, por lo que la fuerza de interacción entre partículas es uno de los factores clave de la dispersión.
Teoría de la doble capa eléctrica
La teoría de la doble capa eléctrica se puede utilizar para explicar la distribución de iones cargados en los coloides y los posibles problemas en la superficie de las partículas. En el siglo XIX, Helmholtz propuso el modelo de condensadores paralelos para describir la estructura de doble capa eléctrica. Simplemente se supone que las partículas tienen carga negativa y la superficie es como un electrodo en un capacitor. Sin embargo, esta teoría ignora el comportamiento de difusión de los iones cargados debido al movimiento térmico.
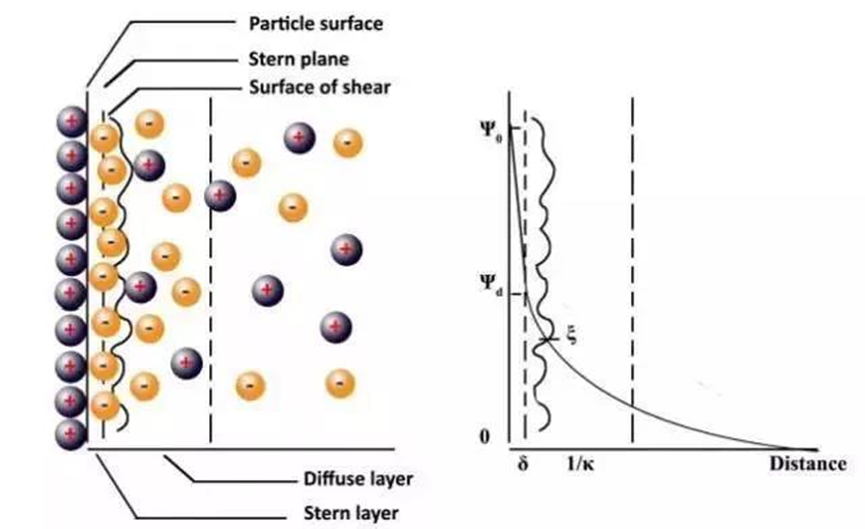
Por lo tanto, a principios del siglo XX, Gouy y Chapman propusieron el modelo de doble capa eléctrica de difusión, en el que los contraiones en solución se adsorberán en la superficie de las partículas cargadas debido a la interacción electrostática y, al mismo tiempo, difundir alrededor de las partículas debido al movimiento térmico. Por lo tanto, la concentración de distribución de contraiones en la solución disminuirá con la distancia desde la superficie de la partícula. En 20, Stern combinó los dos modelos de condensador paralelo y doble capa eléctrica difusa para describir la estructura de la doble capa eléctrica. Stern cree que los contraiones formarán una capa de adsorción apretada en la superficie de la partícula, también conocida como capa de Stern. A medida que aumenta la distancia desde la superficie de la partícula, el potencial de la partícula disminuirá linealmente. Al mismo tiempo, también hay una capa de difusión fuera de la capa de Stern, y las partículas se difundirán. El potencial en la capa disminuye exponencialmente con la distancia.
La siguiente figura muestra el modelo eléctrico de doble capa de Stern. El potencial zeta (ξ, potencial Zeta) es un parámetro muy importante en el modelo de doble capa eléctrica. El potencial de superficie de la partícula no se puede medir directamente en la medición real, pero se puede calcular mediante el método de ondas acústicas o el método de electroforesis. el potencial zeta de la partícula. El potencial zeta existe en el plano de corte entre la capa de Stern y la capa de difusión en el modelo de doble capa eléctrica.
El potencial zeta está estrechamente relacionado con la estabilidad de dispersión del coloide. Cuando el potencial zeta es mayor, la carga electrostática en la superficie de la partícula coloidal es mayor. Cuando el potencial zeta de la partícula en la solución acuosa alcanza ±25~30mV, el coloide tiene suficiente repulsión electrostática para vencer las fuerzas de van der Waals entre partículas para mantener la estabilidad coloidal.
teoría DLVO
De 1940 a 1948, Deryagin, Landau, Verwey, Overbeek establecieron la teoría relacionada del cambio de energía cuando las partículas coloidales se acercan entre sí y su influencia en la estabilidad coloidal, denominada teoría DLVO. Su teoría describe principalmente la relación entre la distancia entre las partículas coloidales y el cambio de energía.
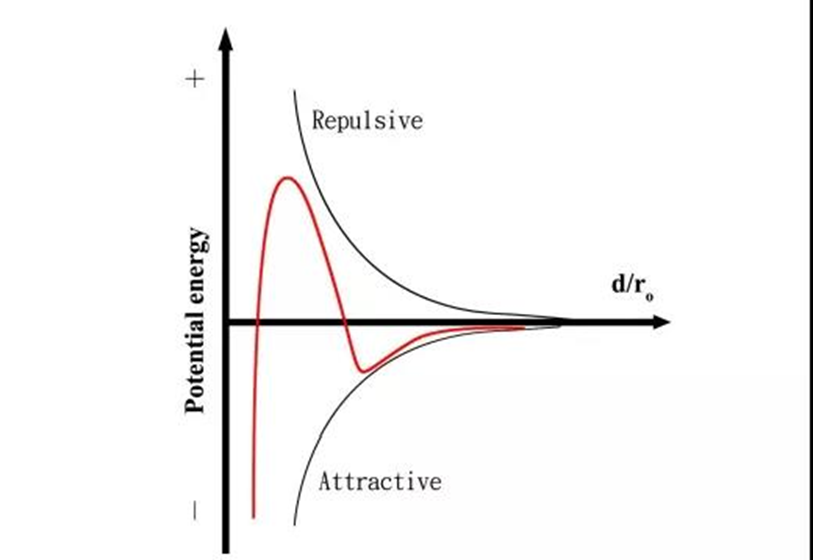
La siguiente figura es un diagrama esquemático de DLVO, que indica que existen fuerzas atractivas y repulsivas entre las partículas coloidales. El tamaño de estas dos fuerzas determina la estabilidad de la solución coloidal. La atracción entre partículas es el efecto principal, y las partículas se aglomerarán; mientras que la fuerza repulsiva en un estado mayor que la fuerza atractiva, se puede evitar la cohesión de la partícula y se puede mantener la estabilidad del coloide.
A partir de la curva DLVO, cuando la distancia entre las partículas es cada vez más corta, las partículas primero se atraerán entre sí, si las partículas continúan acercándose, se generará la fuerza repulsiva entre las partículas, y si las partículas cruzan la Barrera de repulsión, los agregados rápidamente. Por lo tanto, para mejorar la estabilidad de dispersión de partículas en coloides, se debe mejorar la fuerza repulsiva entre partículas para evitar la aglomeración entre partículas.
Mecanismo de estabilización de coloides
Las partículas coloidales tienden a aglomerarse debido a su alta energía superficial. Para que el sistema coloidal tenga estabilidad de dispersión, se debe mejorar la fuerza repulsiva entre partículas. El mecanismo de estabilización entre coloides generalmente se puede dividir en tres tipos:
1) estabilización electrostática
2) Obstáculo estérico
3) Estabilización electrostérica, el mecanismo de estabilización se muestra en la siguiente figura:
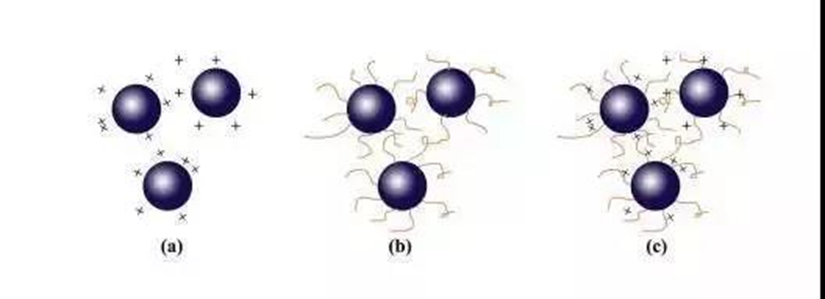
(a) repulsión electrostática, (b) barrera estérica, (c) barrera estérica electrostática
El mecanismo de estabilización electrostática utiliza la fuerza de repulsión provocada por las cargas superficiales de las partículas. Cuando las partículas están cerca unas de otras debido a la atracción, las dobles capas eléctricas de las partículas coloidales se superponen y la fuerza de repulsión se genera debido a la misma carga en la superficie de las partículas.
Sin embargo, el mecanismo de estabilización electrostática se ve fácilmente afectado por la concentración de electrolitos en el sistema de solución. Cuando la concentración de electrolito en la solución es demasiado alta, la doble capa eléctrica en la superficie de las partículas se comprimirá, lo que hará que las partículas se aglomeren. El mecanismo de estabilización de las barreras estéricas consiste en utilizar macromoléculas para adsorberse en la superficie de partículas coloidales, lo que producirá dos efectos diferentes para potenciar la fuerza de repulsión entre partículas:
1) Efecto osmótico
Cuando las dos partículas coloidales están próximas entre sí, el polímero de cadena larga adsorbido en la superficie de las partículas o el polímero residual en la solución se interpondrá entre las partículas. En este momento, el aumento continuo de la concentración de polímero entre las partículas provocará el cambio de la presión osmótica y el medio circundante entrará en las dos partículas coloidales. Entre las partículas, la distancia entre sí se organiza para lograr el efecto de dispersión estable.
2) Efecto de restricción de volumen
Para adsorber la macromolécula en la superficie superior de la partícula, existe una cierta barrera espacial. Cuando la distancia entre las partículas se acorta, debido a que la macromolécula no puede penetrar la partícula, la macromolécula se comprimirá, lo que resultará en un aumento de la energía libre elástica, desplazando así a la partícula y logrando el efecto de dispersión. .
En comparación con los mecanismos de estabilización electrostática, las barreras estéricas poliméricas tienen muchas ventajas. El mecanismo de estabilización electrostática se ve fácilmente afectado por el medio ambiente y pierde su efecto, y no se puede aplicar a entornos con alto contenido de electrolitos o soluciones de sistemas orgánicos.
Sin embargo, las barreras estéricas macromoleculares son relativamente insensibles a la concentración de electrolitos y tienen la misma eficacia en solución acuosa o en disolventes orgánicos, y las barreras estéricas macromoleculares no afectan el efecto debido al contenido de sólidos coloidales. Cuando el polímero se adsorbe en la superficie de las partículas coloidales, incluso si se produce la aglomeración, sigue siendo una aglomeración suave, que puede romper fácilmente el fenómeno de la aglomeración. Incluso si las partículas coloidales se secan, aún se pueden dispersar en el solvente nuevamente.
Por lo tanto, el efecto de las barreras estéricas sobre la estabilidad de la dispersión es relativamente mayor que el de la estabilización electrostática. La estabilización estérica electrostática tiene tanto un mecanismo de estabilización electrostática como una barrera estérica. El polímero injertado en la superficie de la partícula se carga, de modo que se suman los dos mecanismos de estabilización diferentes, de manera que las partículas coloidales tienen una buena estabilidad de dispersión.
Gama de productos de Keheng New Energy
- Habilitación de calentamiento a baja temperatura de 100 AH y 12 V
- Célula de batería de litio
- Paquete de baterías de litio
- Batería de scooter/bicicleta eléctrica
- Batería Lifepo12 de 24V/4V
- Estación de energía portátil
- Sistemas de almacenamiento de energía ESS
- Baterías de ciclo profundo con BMS
- Batería de baja temperatura 24V 60AH