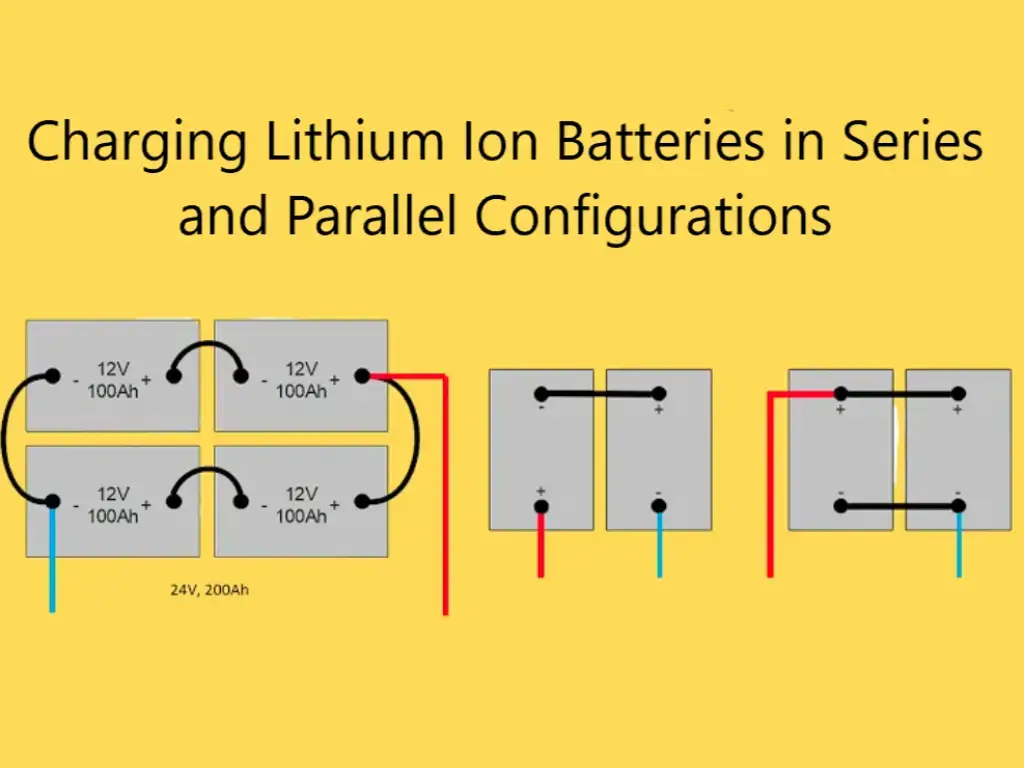
يعد تحريك ملاط خلية بطارية الليثيوم هو الرابط الأكثر أهمية في عملية الإنتاج بأكملها ، وهو الرابط الأكثر أهمية في عملية الإنتاج الكاملة لبطارية أيون الليثيوم.
تكوين ملاط القطب الموجب لبطارية أيون الليثيوم
يتكون ملاط القطب الموجب لبطارية أيون الليثيوم من مادة رابطة ، وعامل موصل ، ومواد قطب موجبة ، وما إلى ذلك ؛ يتكون ملاط القطب السالب من مادة رابطة ومسحوق كربون الجرافيت وما إلى ذلك. يتضمن تحضير الملاط الموجب والسالب سلسلة من العمليات التكنولوجية مثل الخلط المتبادل والذوبان والتشتت بين المواد السائلة والسائلة والسائلة والصلبة ، وهذه العمليات هي مصحوبة بتغيرات في درجة الحرارة واللزوجة والبيئة. في ملاط الإلكترود الموجب والسالب ، يؤثر تشتت المادة الفعالة الحبيبية وتوحيدها بشكل مباشر على حركة أيونات الليثيوم بين قطبي البطارية ، وبالتالي فإن خلط وتشتت ملاط كل مادة قطعة قطب مهم جدًا في إنتاج بطاريات الليثيوم أيون. ، تؤثر جودة تشتت الطين بشكل مباشر على جودة إنتاج بطاريات الليثيوم أيون اللاحقة وأداء منتجاتها.
في العملية التقليدية ، يتم إجراء تشتت فائق الدقة لأنه: من خلال معدات الخلط والتقليب التقليدية ، يمكن فقط تشتيت مجموعات المسحوق الكبيرة في المحلول وتوزيعها بالتساوي ؛ ومع ذلك ، فإن شكل المسحوق موجود في شكل عناقيد مسحوق ناعم. في الحل ، يتم تلبية متطلبات معالجة التشتت العياني فقط. يمكن أن يؤدي الملاط بعد التحريك والتشتت العياني إلى تشتيت وتجانس المسحوق الناعم أو تكتلات الجسيمات الصلبة في المحلول تحت تأثير قوة القطع الميكانيكية القوية لمعدات التشتيت والتجانس فائقة الدقة للحصول على مواد صلبة دقيقة بدرجة كافية. يتم توزيع الجسيمات بشكل موحد في المحلول لتحقيق تأثير التشتت الدقيق للغاية والتجانس ، والذي يمكن أن يحسن بشكل كبير الأداء الشامل للملاط.
عملية ملاط بطارية الليثيوم التقليدية الحالية هي:
المكونات
- تحضير الحل:
أ) نسبة الخلط ووزن PVDF (أو CMC) والمذيبات NMP (أو الماء منزوع الأيونات) ؛
ب) وقت التحريك ، وتكرار التحريك وأوقات المحلول (ودرجة حرارة سطح المحلول) ؛
ج) بعد الانتهاء من تحضير المحلول ، يتم فحص المحلول: اللزوجة (الاختبار) ، ودرجة الذوبان (الفحص البصري) ووقت التخزين ؛
د) القطب السالب: محلول SBR + CMC ، وقت التحريك والتردد.
المواد الفعالة:
أ) عند الوزن والخلط ، يجب مراقبة ما إذا كانت نسبة الخلط والكمية صحيحة ؛
ب) طحن الكرة: وقت طحن الكرة للأقطاب الموجبة والسالبة ؛ نسبة حبات العقيق إلى الخليط في برميل طحن الكرة ؛ نسبة الكرات الكبيرة إلى الكرات الصغيرة في كرات العقيق ؛
ج) الخبز: تحديد درجة حرارة الخبز والوقت ؛ اختبر درجة الحرارة بعد التبريد بعد الخبز.
د) خلط وتحريك المادة الفعالة والمحلول: وضع التحريك ، وقت التحريك والتردد.
ه) المنخل: يمر عبر 100 شبكة (أو 150 شبكة) منخل جزيئي.
و) الاختبار والتفتيش:
يتم إجراء الاختبارات التالية على الملاط والمزيج: المحتوى الصلب واللزوجة ودقة الخلط وكثافة الحنفية وكثافة الملاط.
بالإضافة إلى توضيح الحرفية التقليدية ، من الضروري أيضًا فهم المبادئ الأساسية لملاط بطارية الليثيوم.
نظرية الغروانية
التأثير الرئيسي المؤدي إلى تكتل الجسيمات الغروية هو من قوة فان دير فال بين الجسيمات. لزيادة ثبات الجسيمات الغروية ، هناك طريقتان: الأولى هي زيادة التنافر الكهروستاتيكي بين الجسيمات الغروية ، والأخرى هي توليد إمكانات ستريكية بين المساحيق. بهاتين الطريقتين ، يتم حظر تكتل المسحوق.
أبسط نظام غرواني يتكون من مرحلة مشتتة ووسط مشتت ، ويتراوح حجم المرحلة المشتتة من 10-9 إلى 10-6 م. المواد الموجودة في الغروانية موجودة في النظام وتحتاج إلى درجة معينة من التشتت. وفقًا لاختلاف الطور المذيب والمشتت ، يمكن إنتاج أشكال غروانية مختلفة ، مثل: الضباب عبارة عن رذاذ يتم فيه تشتيت القطرات في الغاز ، ومعجون الأسنان هو محلول غرواني حيث تتشتت جزيئات البوليمر الصلبة في سائل.
يزخر تطبيق الغرويات بالحياة ، وتختلف الخصائص الفيزيائية للغرويات تبعًا لمرحلة التشتت ووسط التشتت. مراقبة الغرويات من وجهة نظر مجهرية ، فإن الجسيمات الغروية ليست في حالة ثابتة ، ولكنها تتحرك بشكل عشوائي في الوسط ، وهو ما نسميه الحركة البراونية. فوق الصفر المطلق ، ستخضع الجسيمات الغروية للحركة البراونية بسبب الحركة الحرارية ، وهي الخصائص الديناميكية للغرويات المجهرية. يعتبر اصطدام الجسيمات الغروية بسبب الحركة البراونية فرصة للتجمع ، والجسيمات الغروية في حالة غير مستقرة من الناحية الديناميكية الحرارية ، وبالتالي فإن قوة التفاعل بين الجسيمات هي أحد العوامل الرئيسية للتشتت.
نظرية الطبقة المزدوجة الكهربائية
يمكن استخدام نظرية الطبقة المزدوجة الكهربائية لشرح توزيع الأيونات المشحونة في الغرويات والمشكلات المحتملة على سطح الجسيمات. في القرن التاسع عشر ، اقترح هيلمهولتز نموذج المكثف المتوازي لوصف هيكل الطبقة المزدوجة الكهربائية. من المفترض ببساطة أن الجسيمات مشحونة سالبة ، والسطح يشبه قطب كهربائي في مكثف. ومع ذلك ، تتجاهل هذه النظرية سلوك انتشار الأيونات المشحونة بسبب الحركة الحرارية.
لذلك ، في بداية القرن العشرين ، اقترح Gouy و Chapman نموذج انتشار الطبقة المزدوجة الكهربائية ، حيث سيتم امتصاص الأيونات المضادة في المحلول على سطح الجسيمات المشحونة بسبب التفاعل الكهروستاتيكي ، وفي نفس الوقت ، سوف تنتشر حول الجسيمات بسبب الحركة الحرارية. لذلك ، سينخفض تركيز توزيع الأيونات المضادة في المحلول مع المسافة من سطح الجسيم. في عام 20 ، جمع ستيرن بين نموذجين للمكثف المتوازي وطبقة مزدوجة كهربائية منتشرة لوصف هيكل الطبقة المزدوجة الكهربائية. يعتقد ستيرن أن الأيونات المضادة ستشكل طبقة امتصاص محكمة على سطح الجسيم ، تُعرف أيضًا باسم طبقة ستيرن. مع زيادة المسافة من سطح الجسيم ، ستنخفض إمكانات الجسيم خطيًا. في الوقت نفسه ، توجد أيضًا طبقة انتشار خارج طبقة ستيرن ، وستنتشر الجسيمات. تتناقص الإمكانات في الطبقة بشكل كبير مع المسافة.
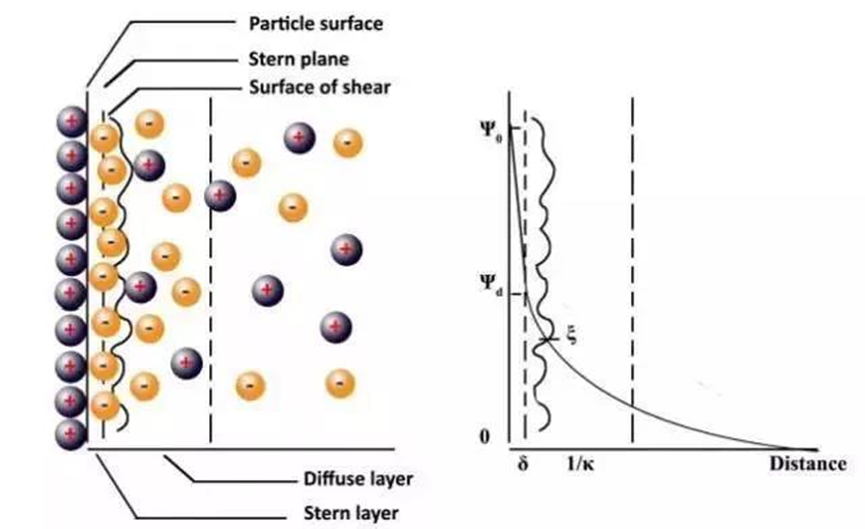
يوضح الشكل أدناه نموذج الطبقة المزدوجة الكهربائي Stern. تعد إمكانات زيتا (ξ ، إمكانات زيتا) معلمة مهمة جدًا في نموذج الطبقة المزدوجة الكهربائية. لا يمكن قياس الإمكانات السطحية للجسيم مباشرة في القياس الفعلي ، ولكن يمكن حسابها بطريقة الموجة الصوتية أو طريقة الرحلان الكهربائي. من إمكانات زيتا للجسيم. توجد إمكانات زيتا على مستوى القص بين طبقة ستيرن وطبقة الانتشار في نموذج الطبقة المزدوجة الكهربائية.
ترتبط إمكانات زيتا ارتباطًا وثيقًا باستقرار تشتت الغروانية. عندما تكون إمكانات زيتا أكبر ، تكون الشحنة الكهروستاتيكية على سطح الجسيم الغرواني أكثر. عندما تصل إمكانات زيتا للجسيم في المحلول المائي إلى ± 25 ~ 30 مللي فولت ، يكون للغرواني تنافر إلكتروستاتيكي كافٍ يتغلب على قوى فان دير فال بين الجسيمات للحفاظ على الاستقرار الغرواني.
نظرية DLVO
من عام 1940 إلى عام 1948 ، أسس Deryagin ، Landau ، Verwey ، Overbeek النظرية ذات الصلة لتغير الطاقة عندما تقترب الجسيمات الغروية من بعضها البعض وتأثيرها على الاستقرار الغرواني ، المشار إليها باسم نظرية DLVO. تصف نظريتها بشكل أساسي العلاقة بين المسافة بين الجسيمات الغروية وتغير الطاقة.
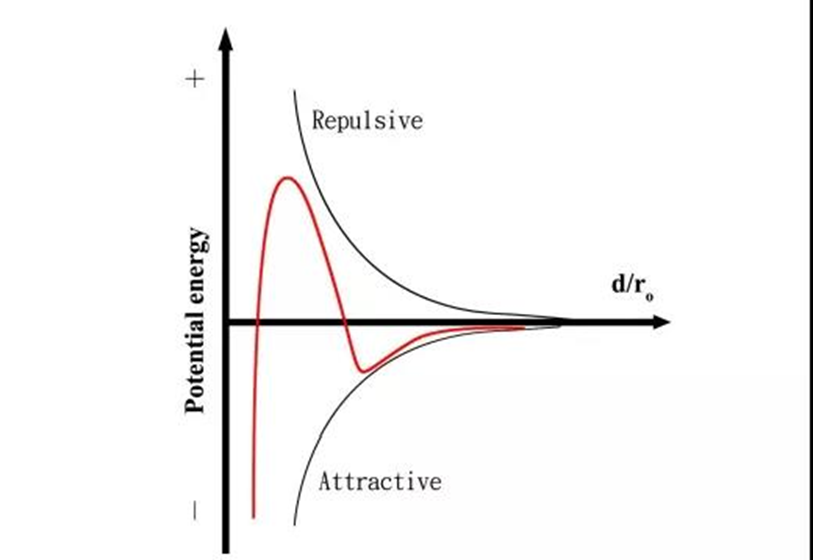
الشكل التالي هو رسم تخطيطي لـ DLVO ، مما يشير إلى وجود قوى جذابة ومنافرة بين الجسيمات الغروية. يحدد حجم هاتين القوتين استقرار المحلول الغرواني. التأثير الرئيسي هو التجاذب بين الجسيمات ، وسوف تتكتل الجسيمات ؛ بينما القوة الطاردة في حالة أكبر من القوة الجذابة ، يمكن تجنب تماسك الجسيمات ويمكن الحفاظ على استقرار الغروانية.
من منحنى DLVO ، عندما تصبح المسافة بين الجسيمات أقصر وأقصر ، سوف تجذب الجسيمات بعضها البعض أولاً ، إذا استمرت الجسيمات في الاقتراب من بعضها البعض ، فسيتم إنشاء القوة الطاردة بين الجسيمات ، وإذا عبرت الجسيمات بعضها البعض حاجز التنافر ، يتجمّع بسرعة. لذلك ، من أجل تحسين استقرار تشتت الجزيئات في الغرويات ، يجب تحسين قوة التنافر بين الجسيمات لتجنب التكتل بين الجسيمات.
آلية استقرار الغروانية
تميل الجسيمات الغروية إلى التكتل بسبب طاقتها السطحية العالية. من أجل جعل النظام الغرواني يتمتع باستقرار تشتت ، يجب تحسين قوة التنافر بين الجسيمات. يمكن تقسيم آلية التثبيت بين الغرويات عمومًا إلى ثلاثة أنواع:
1) الاستقرار الالكتروستاتيكي
2) عائق ستيري
3) التثبيت الكهربائي ، تظهر آلية التثبيت في الشكل التالي:
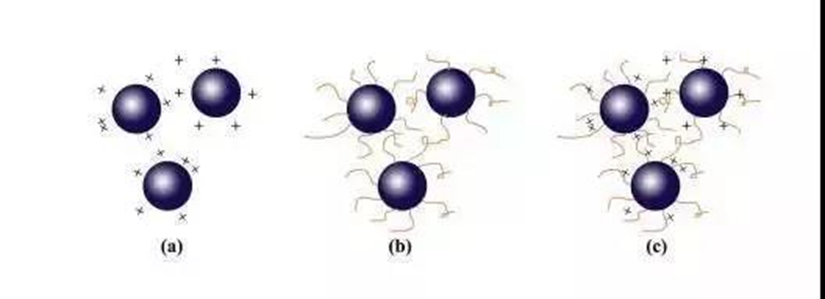
(أ) التنافر الإلكتروستاتيكي ، (ب) الحاجز الفراغي ، (ج) الحاجز الإستاتيكي الكهروستاتيكي
تستخدم آلية التثبيت الكهروستاتيكي القوة الطاردة التي تسببها الشحنات السطحية للجسيمات. عندما تكون الجسيمات قريبة من بعضها البعض بسبب التجاذب ، تتداخل الطبقات الكهربائية المزدوجة للجسيمات الغروانية ، وتتولد قوة التنافر بسبب نفس الشحنة على سطح الجسيمات.
ومع ذلك ، فإن آلية التثبيت الكهروستاتيكي تتأثر بسهولة بتركيز الإلكتروليت في نظام المحلول. عندما يكون تركيز الإلكتروليت في المحلول مرتفعًا جدًا ، سيتم ضغط الطبقة المزدوجة الكهربائية الموجودة على سطح الجزيئات ، مما يؤدي إلى تكتل الجسيمات. تتمثل آلية تثبيت الحواجز الستريكية في استخدام الجزيئات الكبيرة للامتصاص على سطح الجسيمات الغروية ، مما ينتج عنه تأثيران مختلفان لتعزيز قوة التنافر بين الجسيمات:
1) التأثير الأسموزي
عندما يقترب الجسيمان الغروانيان من بعضهما البعض ، فإن البوليمر طويل السلسلة الممتص على سطح الجسيمات أو البوليمر المتبقي في المحلول سيتم تداخله بين الجسيمات. في هذا الوقت ، ستؤدي الزيادة المستمرة في تركيز البوليمر بين الجزيئات إلى تغيير الضغط الاسموزي ، وسيدخل الوسط المحيط الجسيمين الغروانيين. بين الجسيمات ، يتم ترتيب المسافة من بعضها البعض لتحقيق تأثير التشتت المستقر.
2) تأثير تقييد الحجم
من أجل امتصاص الجزيء الكبير على السطح العلوي للجسيم ، هناك حاجز فضاء معين. عندما يتم تقصير المسافة بين الجسيمات ، لأن الجزيء الكبير لا يستطيع اختراق الجسيم ، سيتم ضغط الجزيء الكبير ، مما يؤدي إلى زيادة الطاقة الحرة المرنة ، وبالتالي إزاحة الجسيم وتحقيق تأثير التشتت. .
بالمقارنة مع آليات التثبيت الكهروستاتيكي ، فإن الحواجز الستريكية البوليمرية لها العديد من المزايا. تتأثر آلية التثبيت الكهروستاتيكي بسهولة بالبيئة وتفقد تأثيرها ، ولا يمكن تطبيقها على البيئات عالية الإلكتروليت أو حلول النظام العضوي.
ومع ذلك ، فإن الحواجز الفراغية الجزيئية غير حساسة نسبيًا لتركيز الإلكتروليت ، ولها نفس الكفاءة في المحلول المائي أو في المذيبات العضوية ، ولا تؤثر الحواجز الفراغية الجزيئية الكبيرة على التأثير بسبب المحتوى الصلب الغرواني. عندما يتم امتصاص البوليمر على سطح الجسيمات الغروية ، حتى في حالة حدوث التكتل ، فإنه لا يزال يتكتل لينًا ، والذي يمكنه بسهولة كسر ظاهرة التكتل. حتى إذا جفت الجزيئات الغروية ، فلا يزال من الممكن تشتيتها في المذيب مرة أخرى.
لذلك ، فإن تأثير الحواجز الساكنة على استقرار التشتت أعلى نسبيًا من تأثير التثبيت الكهروستاتيكي. يحتوي التثبيت الكهروستاتيكي الثابت على آلية استقرار كهروستاتيكي وحاجز ثابت. يتم شحن البوليمر المطعوم على سطح الجسيم ، بحيث تتم إضافة آليتي التثبيت المختلفتين ، بحيث تتمتع الجسيمات الغروانية باستقرار تشتت جيد.
مجموعة منتجات Keheng New Energy
- 100AH 12 فولت تدفئة منخفضة الحرارة تمكينâ € <
- خلية بطارية الليثيوم
- حزمة بطارية الليثيوم
- بطارية Escooter / Ebike
- بطارية Lifepo12 24V / 4V
- محطة الطاقة المحمولة
- أنظمة تخزين الطاقة ESS
- بطاريات الدورة العميقة مع BMS
- بطارية منخفضة الحرارة 24 فولت 60 أمبير